(UroToday.com) На ежегодном собрании Американского общества клинической онкологии (ASCO) 2024 года, проходившем в Чикаго, штат Иллинойс, прошла постерная сессия, посвященная исследованиям рака простаты, яичек и полового члена. Доктор Карим Физази представил исследование III фазы MK-5684-004, сравнивающее MK-5684, ингибитор CYP11A1, с гормональным препаратом нового поколения (NHA) у пациентов с метастатическим кастрационно-резистентным раком простаты (мКРРПЖ) после однократного предшествующего прогрессирования. . Ноха.
Активирующие соматические мутации андрогенного рецептора (АР) являются распространенным механизмом устойчивости к АР-направленной терапии при мКРРПЖ и могут способствовать сохранению гормональной зависимости. Вышестоящее нацеливание на биосинтез андрогенов может обеспечить терапевтическое преимущество перед доступными анти-АР-терапией мКРРПЖ. Убивисостат (МК-5684; ОДМ-208) представляет собой пероральный нестероидный ингибитор цитохрома Р450 11А1 (CYP11A1), который катализирует начальную и лимитирующую стадию биосинтеза стероидов. Ингибирование CYP11A1 обивизостатом может ингибировать выработку всех стероидных гормонов и их предшественников, которые могут беспорядочно активировать сигнальный путь AR. В фазе 1/2 исследования CYPIDES убивисостат продемонстрировал противоопухолевую активность у пациентов с предварительно получавшим интенсивное лечение мКРРП, особенно у пациентов с мутациями AR-связывающего домена (AR-LBD).1 В открытом рандомизированном исследовании III фазы MK-5684-004 (NCT06136650) будет оцениваться эффективность и безопасность убивисостата по сравнению с переключаемым NHA у пациентов с молекулярно неселектированным мКРРПЖ после предшествующей терапии NHA.
Дизайн исследования кратко изложен ниже. В этом исследовании 1500 пациентов с мКРРПЖ, не отобранных по мутациям AR-LBD, с прогрессирующим заболеванием во время или после NHA по поводу гормоночувствительного рака простаты (метастатического или неметастатического) или неметастатического 1:1 будут рандомизированы в одну группу:
- Группа 1: обивизостат 5 мг перорально два раза в день + дексаметазон 1,5 мг и флудрокортизон 0,1 мг перорально один раз в день.
- Рычаг 2: переключатель NHA
- Абиратерона ацетат 1000 мг перорально один раз в день + преднизолон 5 мг перорально два раза в день или энзалутамид 160 мг перорально один раз в день
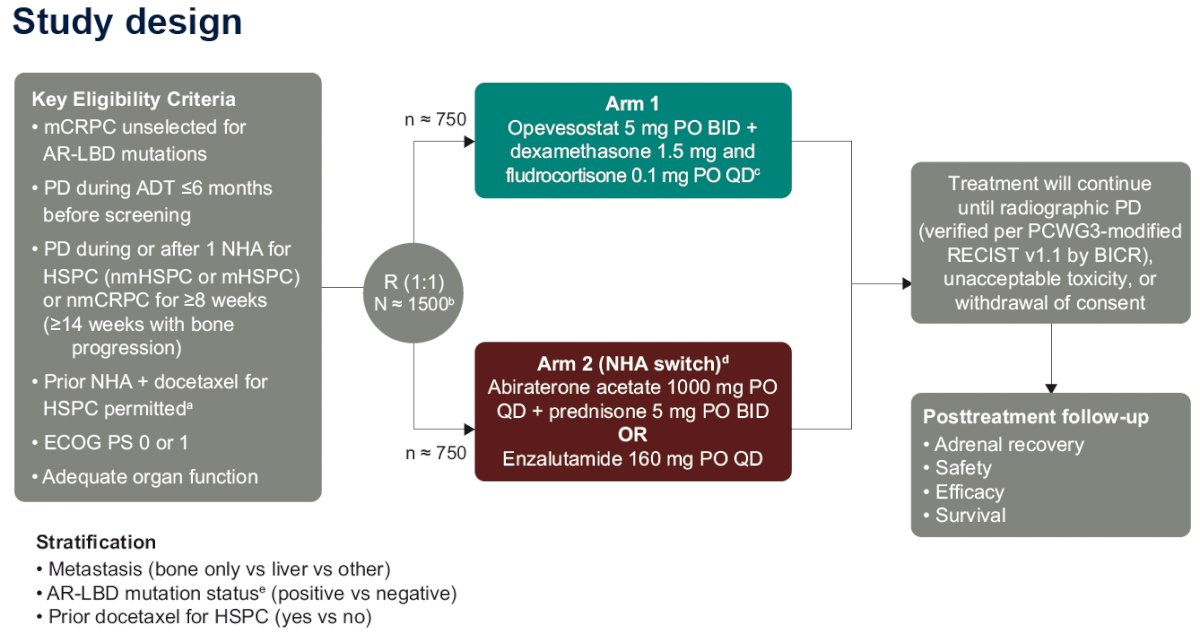
Основные критерии отбора приведены в таблице ниже:
Основная цель исследования — оценить следующее для обивизостата по сравнению с абиратерона ацетатом или энзалутамидом у пациентов с мутацией AR-LBD и AR-отрицательным мКРРПЖ, отдельно:
- Рентгенографическая выживаемость без прогрессирования (rPFS) согласно модифицированной Рабочей группой 3 по клиническим исследованиям рака простаты (PCWG3) версии 1.1 RECIST, проведенной слепым независимым центральным обзором (BICR)
- Общая выживаемость (ОС)
Вторичные результаты следующие:
- Время от рандомизации до начала первого последующего противоракового лечения или смерти (TFST)
- Частота объективного ответа (ЧОО) и продолжительность ответа (ДОР) согласно PCWG3-скорректированному RECIST v1.1 от BICR у пациентов с измеримым заболеванием
- Время до прогрессирования боли (TTPP; время от рандомизации до прогрессирования боли, как определено в пункте 3 Краткого опросника боли – краткая форма). [BPI-SF] И по баллу алгоритма количественной оценки жилья)
- Изменение исходного уровня, время до ухудшения (TTD) и общее улучшение показателей подшкалы функциональной оценки общей терапии рака (FACT-G) и подшкалы функциональной оценки рака простаты (FACT-P).
- Время до развития простатспецифического антигена (ПСА) (время от рандомизации до даты развития ПСА)
- Частота ответа на ПСА (снижение уровня ПСА на ≥50% по сравнению с исходным уровнем, измеренное дважды с интервалом в 3 недели)
- Время до первого события, связанного со скелетом (SSE; время от рандомизации до первого возникновения SSE)
- Безопасность и выносливость
Оценка исследования и последующее наблюдение будут проводиться следующим образом:
Текущий статус исследования следующий:
Представлено: Карим Физази, доктор медицинских наук, профессор медицинского факультета Института Гюстава Русси, Париж, Франция
Автор: Рашид Сайед, доктор медицинских наук, магистр наук, клинический научный сотрудник Общества урологической онкологии (SUO) Университета Торонто, @rksayyid в Твиттере во время ежегодного собрания Американского общества клинической онкологии (ASCO) 2024 года, Чикаго, Иллинойс, пятница , 31 мая – вторник, 4 июня 2024 г.
ссылка:
- Физзази К., Бернар-Тессье А., Рубо Дж. и др. Направленное ингибирование CYP11A1 при кастрационно-резистентном раке простаты. Гид Наджима. 2024;3:EVIDoa2300171.

«Главный евангелист пива. Первопроходец в области кофе на протяжении всей жизни. Сертифицированный защитник Твиттера. Интернетоголик. Практикующий путешественник».








More Stories
Ученые раскрыли секреты потери морских звезд и возобновления роста конечностей
Комплексное мероприятие сообщества людей с деменцией в Ратуте, посвященное Всемирному месяцу борьбы с болезнью Альцгеймера.
Новое исследование массивного надвига предполагает, что следующее большое землетрясение может быть неизбежным