Недавние исследования в области неврологии постоянно указывают на роль гена C9ORF72 в развитии некоторых нейродегенеративных заболеваний. Эти исследования показали, что мутации в этом гене увеличивают риск развития бокового амиотрофического склероза (БАС) и лобно-височной деменции (ЛВД), двух нейродегенеративных заболеваний, характеризующихся двигательными нарушениями, проблемами общения и другими характерными симптомами.
Исследователи из Медицинской школы Университета Джона Хопкинса, Чикагского университета, Медицинского института Говарда Хьюза и других институтов США недавно провели исследование, направленное на лучшее понимание процессов, посредством которых мутация гена C9ORF72 может способствовать развитию БАС и ЛВД. Их выводы, опубликованные в Естественная неврологиявыдвигая на первый план многообещающий метод, который может улучшить терапевтические вмешательства для этих сложных нейродегенеративных расстройств.
«Моя исследовательская группа была заинтересована в изучении скорости метаболизма повторяющейся РНК C9ORF72», — сказал Medical Xpress доктор Шуин Сунь, один из исследователей, проводивших исследование. «Экспансия гексануклеотидных повторов в гене C9ORF72 является наиболее распространенной генетической причиной как БАС, так и ЛВД. Поскольку экспансия расположена в некодирующей области, считается, что одиночная повторная РНК является основным фактором патогенеза».
Сан и ее коллеги пытаются идентифицировать генетические модификаторы для нетрадиционного производства токсичных полипептидных белков из повторяющихся РНК. Это, в свою очередь, может позволить им определить жизнеспособные стратегии для предотвращения накопления этих токсичных белков и, таким образом, уменьшить их токсическое действие. В одном из своих предыдущих исследований они провели полногеномный скрининг CRISPR-Cas9 для поиска генетических модификаторов производства дипептидов.
Мы обнаружили, что два М6Сан объяснил, что метилтрансферазы являются генами-кандидатами, которые могут модулировать уровень полипептидного дипептида. Мы также проанализировали общие протеомные данные и обнаружили, что две метилтрансферазы активируются в нейронах C9ORF72-ALS/FTD iPS пациентов. В целом, это положило начало нашему дальнейшему изучению М.6Нарушение регуляции и то, как это способствует нейродегенерации при C9ORF72-ALS/FTD. »
Сан и его коллеги провели серию анализов индуцированных пациентом плюрипотентных нейронов (ИПСК) и посмертных тканей, извлеченных из умерших пациентов с БАС/ЛВД и мутациями гена C9ORF72. Используя технологии высокопроизводительного геномного секвенирования, они специально оценили модифицированную РНК, известную как M.6A (метиладенозин) и его влияние на регуляцию генов во всем диапазоне экспрессируемых матричных РНК (мРНК), известных как транскриптом.
«Мы также изучили молекулярный механизм M6Сунь сказал, что специфичная для репликации C9 регуляция РНК. Наконец, мы измерили выживаемость нейронов, чтобы изучить эффективность спасения, модифицировав m6дорога. Наши результаты раскрывают новый уровень регуляции РНК, который играет критическую роль в патогенном механизме, лежащем в основе нейродегенерации. »
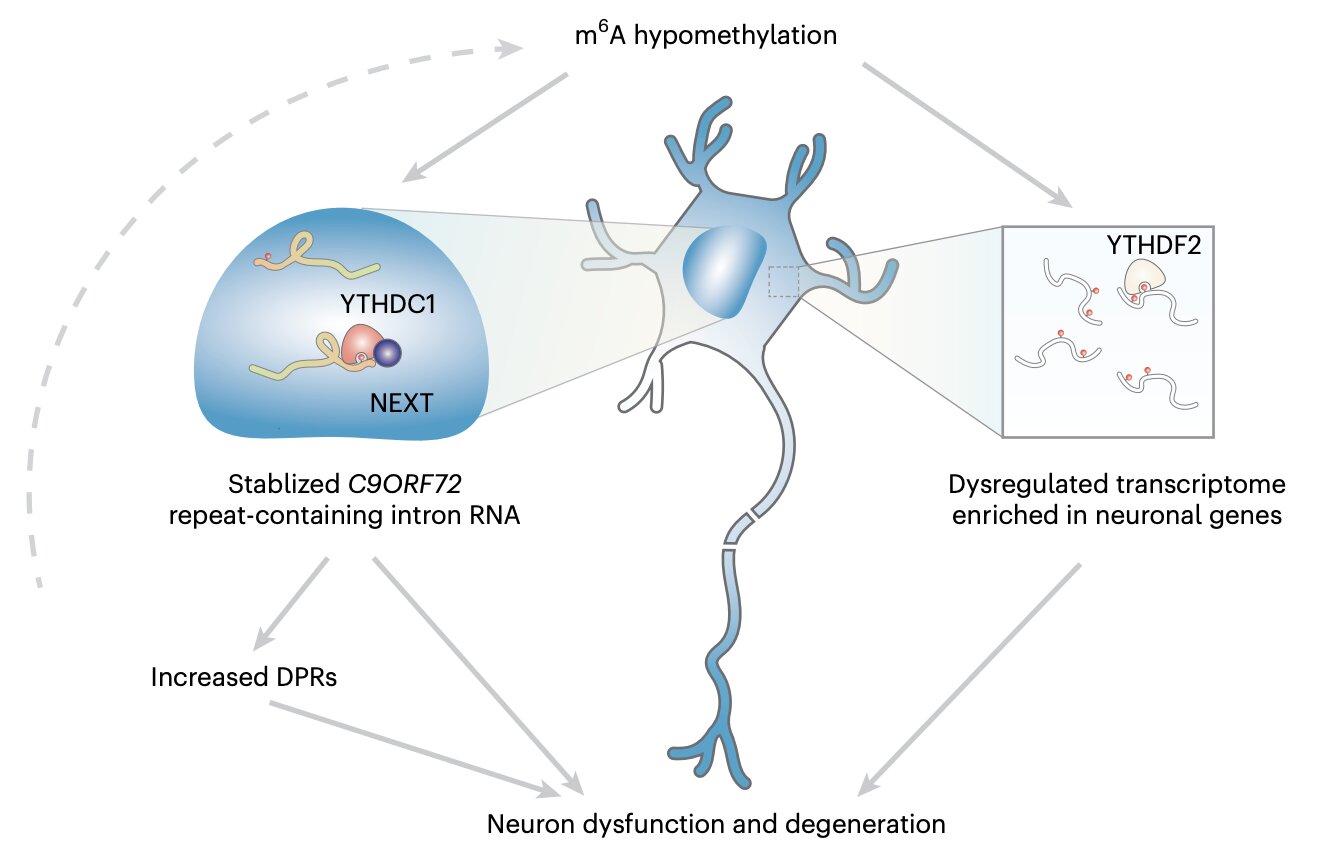
В целом, результаты, собранные этой исследовательской группой, показали, что M6Модификация геномной последовательности расширенных повторов C9ORF72 облегчает деградацию РНК через ядерный ридер YTHDC1, тем самым регулируя повторы. Кроме того, снижение M6Было показано, что он способствует накоплению повторяющихся РНК и кодирует токсичные белки, которые, как известно, связаны с нейродегенерацией.
Подняв м6Сан и ее коллеги смогли значительно снизить уровень повторной РНК, что защитило нейроны, на которых они экспериментировали, и снизило риск их дегенерации. В будущем эти результаты могут проложить путь к разработке более эффективных методов лечения БАС и ЛВД, например, к стимулирующим испытаниям, оценивающим ценность эпитранскриптомной терапии как потенциального вмешательства.
«Мы хотели бы дополнительно проверить эффективность спасения in vivo с использованием соответствующих моделей мышей», — добавил Сан. «Мы также заинтересованы в разработке фармацевтических подходов, нацеленных на этот путь. Кроме того, мы надеемся исследовать лежащие в основе болезни механизмы, включающие метаболизм РНК и m6Дисфункция при перемежающемся боковом амиотрофическом склерозе и других неврологических расстройствах».
Дополнительная информация:
Yini Li et al. Глобально сниженный уровень N6-метиладенозина (m6A) при C9ORF72-ALS/FTD снижает метаболизм РНК и способствует нейродегенерации, Естественная неврология (2023). DOI: 10.1038/s41593-023-01374-9
© 2023 Наука Х Сеть

«Главный евангелист пива. Первопроходец в области кофе на протяжении всей жизни. Сертифицированный защитник Твиттера. Интернетоголик. Практикующий путешественник».


:quality(70)/cloudfront-eu-central-1.images.arcpublishing.com/irishtimes/TP4BGRQQTBHPXFPV3QQLZU4T2A.jpg)



More Stories
Бактерии, поедающие углерод, могут быть ключом к удалению углерода
Развитие рака кожи, его профилактики и лечения за последний год
Скручивание и связывание волн материи с фотонами в полости